Taking of samples for histopathology and cytology
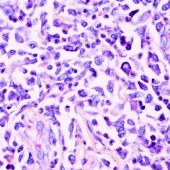
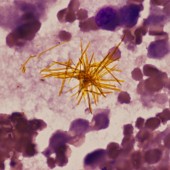
Histopathological examination
Samples of tissue of apropriate size (1-3 cm3) are "fixed" to preserve the cells/tissue in as natural a state as possible and prevent postmortem decay (autolysis and putrefaction). Even the most careful fixation alters the sample to a certain extent and may potentially introduce artifacts that can interfere with interpretation of images of the fine detail of cells, incl. all their organelles, that can only be observed using an electron microscope .
Fixation is usually the first stage in a multistep process to prepare biological material for microscopy or other analysis, the choice of fixation method and specific fixative may depend on the subsequent processing steps appropriate in that particular case.
Chemical fixation
In this case biological structures are preserved in a state as close to that of the living tissue as possible. This requires a chemical fixative that can stabilise the proteins, nucleic acids and mucosubstances of the tissue by making them insoluble. The fixative of choise is 10% buffered formalin. Preparation of this solution is very eaesy. You can bay aprox. 40% formalin in the drugstore. This 40% solution must be diluted ten times i. e. add 9 parts of tap water to one part of 40% formalin. Amount of diluted formalin solution depends on the size of the sample. This should be at least 1:20, i. e. sample of size 1 cm3 (= 1 ml) will be put to the 20 ml of fixative. Time of fixaton is 24 hours and must be send to the pathologist with properly filed request form.
Frozen sections
Small pieces of tissue (typically 5mm x 5mm x 3 mm) are placed in a cryoprotective embedding medium then snap frozen in isopentane (an alkane) cooled by liquid nitrogen. Tissue is then sectioned in a freezing microtome or cryostat. Sections are then fixed by immersion in a specific fixative or series of fixatives for carefully controlled period of time.